Google DeepMindによって開発された高度なアルゴリズムが、生物学における最大の未解決の謎の一つを解き明かしつつある。AlphaFoldは、その構成要素の「指示コード」からタンパク質の3D構造を予測することを目的としている。最新のアップグレードが最近リリースされた。
タンパク質は生物の重要な部分であり、細胞内のほぼすべてのプロセスに関与している。しかし、その形状は複雑であり、視覚化が難しい。そのため、タンパク質の3D構造を予測できることは、生物(人間を含む)内部のプロセスを理解する窓を提供する。
これは、病気を治療するための薬を作成する新たな機会を提供する。これにより、分子医学と呼ばれる分野で新たな可能性が開かれる。分子医学では、科学者たちは分子レベルでの病因を特定し、それを分子レベルで修正する治療法を開発しようとしている。
DeepMindのAIツールの最初のバージョンは2018年に発表された。今年リリースされた最新バージョンはAlphaFold3である。1994年以来、二年ごとに新しいタンパク質構造予測方法を評価する世界的な競技会、構造予測のための重要評価(Casp)が開催されている。2020年には、この競技会でAlphaFold2がテストされ、その性能に非常に感銘を受けた。それ以来、研究者たちはアルゴリズムの新しいバージョンを熱心に待ち望んでいる。
しかし、大学院生として私はかつて、課題でAlphaFold2を使用したことで叱責されたことがある。それは、AlphaFold2が予測ツールに過ぎないと見なされたためである。言い換えれば、実験的な検証なしに、予測されたものが実際のタンパク質と一致するかどうかを誰が知ることができるだろうか?
これは正当なポイントである。実験的な分子生物学の分野も、過去10年間で強力な進展を遂げており、クライオ電子顕微鏡(cryo-EM)という凍結サンプルと穏やかな電子ビームを使用して生体分子の構造を高解像度で捉える技術が革新をもたらしている。
AIツールであるAlphaFoldの利点は、ほぼコストゼロで、タンパク質の構造を非常に迅速に(数分以内に)解明できる点である。結果はオンラインでより簡単にアクセス可能であり、グローバルに利用できる。また、膜タンパク質のように実験的に検証するのが非常に困難なタンパク質の構造も予測できる。
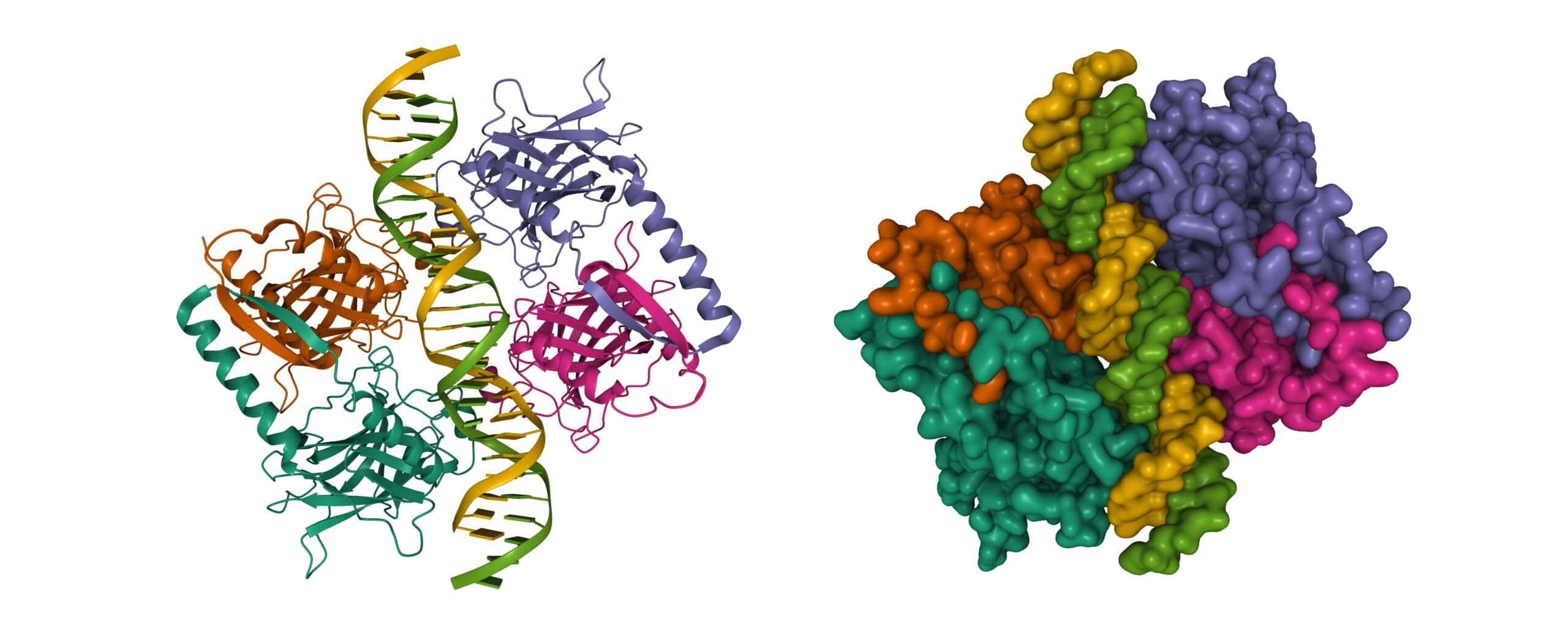
しかし、AlphaFold2は、複数のタンパク質サブユニットが大きなタンパク質を形成する四次構造を扱うようには設計されていなかった。これは、タンパク質分子の異なるユニットがどのように折りたたまれているかの動的な視覚化を伴う。また、一部の研究者は、コイルと呼ばれるタンパク質の構造要素の予測に難しさがあると報告していた。

5月に教授からAlphaFold3がリリースされたとのニュースを伝えられたとき、私の最初の質問は四次構造の予測能力についてであった。成功したのか?完全な構造を予測するための大きな飛躍を遂げたのか?初期の報告では、これらの質問に対する答えは肯定的であると示唆している。
実験的方法は遅い。そして、分子の3D構造を捉えた場合、それは動きや相互作用を伴う体内での行動を見るのではなく、タンパク質の彫像、すなわちスナップショットを見るようなものである。言い換えれば、私たちは写真ではなく映画を求めているのである。
また、膜タンパク質は、伝統的に実験的方法では困難であった。これらは細胞の膜に付着または関連している重要な分子であり、最悪の病気の多くを理解し治療する上で重要である。
ここでAlphaFold3は本当に風景を変えるかもしれない。もし、結晶学、cryo-EMなどの実験的方法に匹敵するかそれを超えるレベルで四次構造を予測でき、膜タンパク質を競合よりもよく視覚化できるなら、私たちは真の分子医学への競争において巨大な飛躍を遂げることになるだろう。
AlphaFold3はDeepMindのサーバーからしかアクセスできないが、使いやすい。研究者は、シーケンスからわずか数分で結果を得ることができる。AlphaFold3のもう一つの約束は、さらなる革新である。DeepMindだけがタンパク質折りたたみ問題の解決を目指しているわけではない。次のCasp競技会が近づく中で、他にも競争に勝つことを目指している人々がいる。例えば、Reading大学のLiam McGuffinとそのチームは、品質評価とタンパク質複合体の化学量論の予測において進展を見せている。化学量論とは、要素や化合物がどのような割合で互いに反応するかを指す。
すべての科学者が同じ方法でこの目標を追い求めているわけではない。他の研究者は、3Dモデルの品質や膜タンパク質が提示する特定の障害など、同様の課題を解決しようとしている。この競争は、この分野の進展にとって素晴らしいものであった。
しかし、実験的方法はすぐに消えることはなく、そうすべきでもない。cryo-EMの進歩は称賛に値し、X線結晶学は今なお生体分子に最高の解像度を提供している。ドイツの欧州XFELレーザーは次のブレークスルーとなる可能性がある。これらの技術は今後も改善され続けるだろう。
この新しい分野を見渡す中で、私が抱く最大の疑問は、絶対的な証拠が得られるまであきらめないという人間の本能がAlphaFoldに屈するかどうかである。この新しい技術が実験的検証に匹敵するかそれを超える結果を提供できるなら、それを受け入れる準備ができているか?もしそうなら、その速度と正確さは、薬の開発などの分野に大きな影響を与える可能性がある。
AlphaFold3によって、タンパク質予測革命の最も重要なハードルを初めてクリアできたかもしれない。この新しい世界をどのように評価し、それでどんな薬を作り出すのか、非常に興味深い。










コメント