冬の到来とともに、寒気と同様に我々の社会を脅かす存在が現れる。インフルエンザである。高熱、節々の痛み、呼吸器症状――これら馴染みのある不快な症状の裏側では、肉眼では決して見ることのできない、極めて微細で劇的なドラマが進行している。
長年、科学者たちはウイルスが細胞に侵入する「その瞬間」を、生きた状態で、かつナノメートルの解像度で目撃することを熱望してきた。これまで、そのプロセスは想像図や、死んだ細胞の静止画をつなぎ合わせることでしか推測できなかったからだ。
しかし、スイス連邦工科大学チューリッヒ校(ETH Zurich)を中心とする国際研究チームが開発した革新的な顕微鏡技術「ViViD-AFM」が、その壁を打ち破った。PNAS(米国科学アカデミー紀要)に発表されたこの研究は、インフルエンザウイルスが細胞膜を「サーフィン」し、細胞がまるでウイルスを歓迎するかのように積極的に取り込む「死の舞踏」の全貌を、世界で初めてリアルタイムで捉えることに成功したのである。
技術的ブレイクスルー:生きた細胞に触れる「最も優しい指」
なぜ、これまでウイルスの侵入を生きたまま観察することが困難だったのか。その理由は、観測技術のジレンマにあった。
従来の電子顕微鏡はナノレベルの解像度を持つが、真空環境が必要であり、観察には細胞を固定(死滅)させる必要があった。一方、生きた細胞を観察できる蛍光顕微鏡は、解像度が低く、ナノスケールの微細な物理的相互作用を捉えるには不十分だった。
ViViD-AFMの誕生
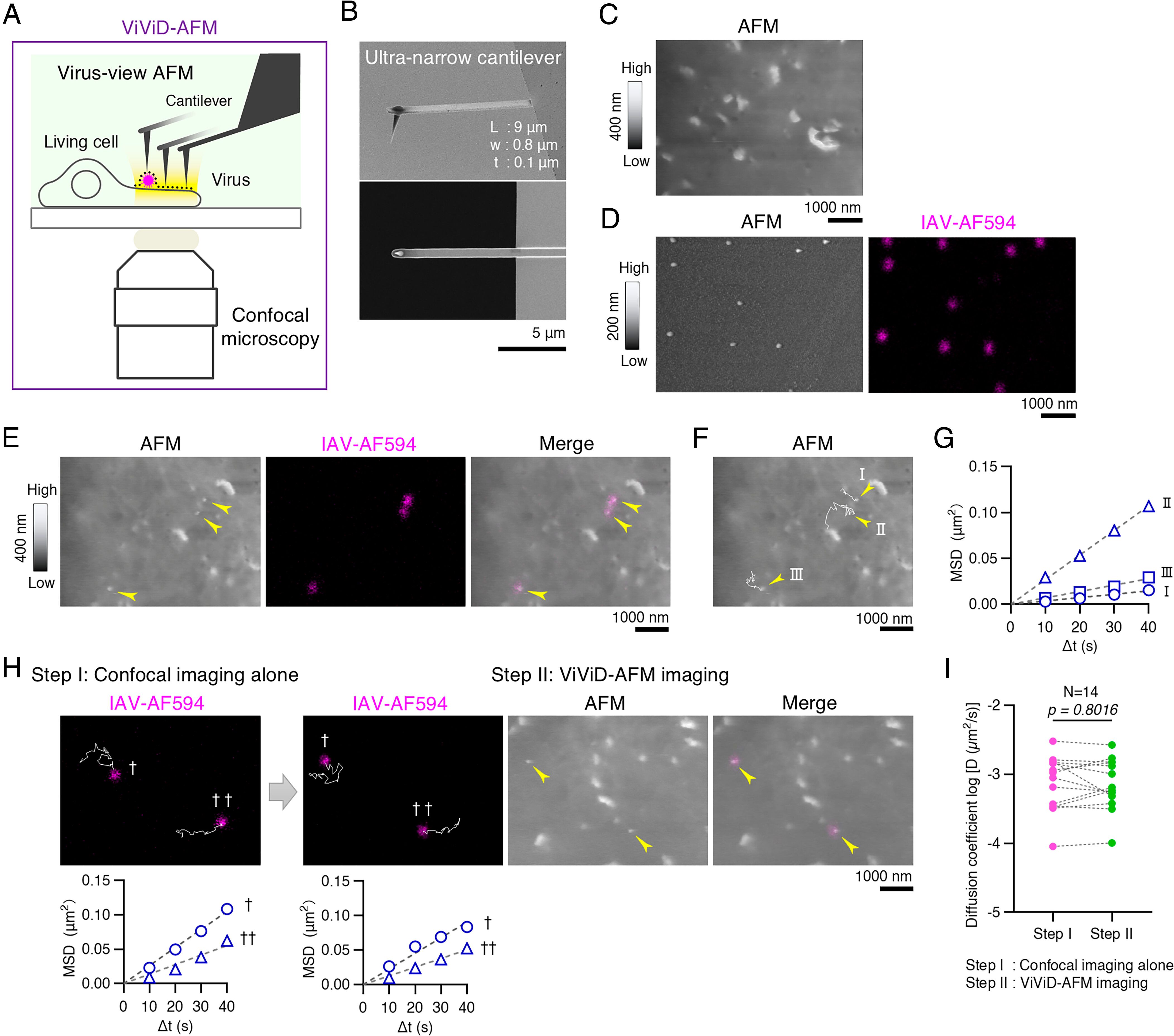
研究チームが開発したViViD-AFM(Virus-View Dual Confocal and Atomic Force Microscopy)は、原子間力顕微鏡(AFM)と共焦点レーザー顕微鏡を高度に融合させたシステムである。
AFMは、極めて鋭利な探針(カンチレバー)で試料の表面をなぞり、その凹凸を原子レベルで画像化する技術だ。しかし、従来のAFMは探針が硬く、柔らかく繊細な動物細胞の膜や、そこに付着するウイルスに対して物理的なダメージを与えてしまう欠点があった。
物理的侵襲性の極小化
本研究の最大の技術的革新は、「超狭小カンチレバー(Ultra-narrow cantilever)」の開発にある。
研究チームは、長さ9.0µm、幅0.8µm、厚さ0.1µmという極微細な探針を設計した。これにより、バネ定数(硬さの指標)を従来の0.1N/mから0.04N/mへと約60%低減させることに成功している。
この改良により、細胞表面にかかる物理的な力(ピークフォース)はわずか10pN(ピコニュートン)に抑えられた。これは、ウイルスと細胞受容体の結合力(10〜25pN)と同等かそれ以下の「優しさ」であり、ウイルスと細胞の結合を破壊することなく、その振る舞いを「生きたまま」「触れて」観察することを可能にしたのである。
ウイルスの「サーフィン」と細胞の「能動的捕獲」
ViViD-AFMによって映し出された映像は、従来の教科書的な理解を覆す驚くべき動態を含んでいた。
1. 細胞膜上のサーフィン
ウイルスは、細胞に到達していきなり侵入するわけではない。まず、細胞表面にあるシアル酸(糖鎖の一種)という「取っ手」を探す。
インフルエンザウイルスの表面には、ヘマグルチニン(HA)とノイラミニダーゼ(NA)という2つのスパイクタンパク質が存在する。HAはシアル酸に結合して細胞にしがみつき、NAは逆にシアル酸を切断して結合を解く役割を持つ。
観察の結果、ウイルスはこの結合(HA)と切断(NA)のバランスを利用し、細胞膜上を滑るように移動していることが判明した。研究チームの山口洋平教授はこの動きを「細胞表面でのサーフィン」と表現している。ウイルスはただ漂っているのではなく、侵入に最適な、受容体が密集した「理想のエントリーポイント」を探してスキャンしているのである。
2. 細胞による「逆」ハイジャック
最も衝撃的な発見は、細胞側の反応であった。従来、細胞はウイルスの侵入に対して受動的な被害者であると考えられがちだった。しかし、ナノスケールの映像が示したのは、細胞が積極的にウイルスを捕まえに行っているという事実だ。
ウイルスが膜上の特定の場所に落ち着くと、細胞はその合図を感知し、細胞骨格タンパク質であるアクチン(Actin)を重合させる。すると、細胞膜の一部が約100nmの高さまで隆起し(バルジ)、ウイルスを包み込むように動き出したのだ。
3. クラスリン被覆ピットの形成
この「抱擁」と並行して、細胞内部ではクラスリン(Clathrin)と呼ばれるタンパク質が集まり、膜を内側に窪ませる準備を始める。
本来、この機構(クラスリン介在性エンドサイトーシス)は、ホルモンや鉄分、コレステロールなど、細胞の生存に必要な栄養素を取り込むための日常的なシステムである。インフルエンザウイルスは、この生命維持に不可欠な輸送システムを巧みに乗っ取り(ハイジャック)、自らを細胞内部へと招き入れさせているのである。
Yamauchi教授が「ウイルスと細胞のダンス」と表現したように、これは一方的な侵略ではなく、ウイルスがリードし、細胞がそれに応えてステップを踏むような、複雑な相互作用の結果であった。
薬理学的介入の可視化:抗ウイルス薬は「ダンス」をどう止めるか
ViViD-AFMの真価は、基礎科学的な発見にとどまらない。この技術は、薬物がウイルスの挙動に与える影響をリアルタイムで評価する強力なツールとなる。
研究チームは、インフルエンザ治療薬であるオセルタミビル(タミフル)を用いた実験も行っている。
- オセルタミビル投与時: ノイラミニダーゼ(NA)の働きが阻害されると、ウイルスがシアル酸から離れられなくなり、膜上での拡散係数(動きやすさ)が有意に低下した。つまり、ウイルスは「サーフィン」ができなくなり、その場に釘付けにされた状態となることが視覚的に確認された。
- シアリダーゼ処理時: 逆に、細胞表面のシアル酸を除去する酵素(シアリダーゼ)を作用させると、ウイルスは結合の手がかりを失い、拡散速度が増加(滑りやすくなる)した。
これらのデータは、ウイルスの拡散速度や膜の変形ダイナミクスを定量的に解析できることを示しており、新薬候補がウイルスの侵入プロセスの「どの段階」を阻害しているのかを、分子レベルで特定できる可能性を示唆している。
静止画から「動画」の時代へ
本研究成果は、ウイルス学および細胞生物学において、以下の3つの重要なパラダイムシフトをもたらすものである。
- 動的メカニズムの解明: これまで「侵入した/しなかった」という結果でしか語られなかった感染プロセスを、時間軸を持った物理現象として解析可能にした。
- 細胞の能動性の証明: 感染成立には、ウイルスの機能だけでなく、細胞側の膜変形(アクチン重合)や陥入(クラスリン集合)といった能動的な協力が不可欠であることを、視覚的かつ定量的に証明した。
- 創薬プラットフォーム: インフルエンザに限らず、他のウイルスや、あるいはドラッグデリバリーシステム(DDS)におけるナノ粒子の細胞内取り込み効率を評価するための、汎用的なプラットフォームとなり得る。
我々は今、ウイルスという不可視の敵が、どのようにして我々の細胞という城塞の門を開けさせているのか、その手口の一部始終を目撃できるようになった。ETH Zurichが開発したこの「新しい眼」は、今後のパンデミック対策やワクチン開発において、極めて重要な役割を果たすことになるだろう。
論文
参考文献
- ETH Zurich: How influenza viruses enter our cells